干细胞疗法有望「唤醒」老年痴呆患者
标签:
每3秒,全球就有一位痴呆症患者产生。而阿尔茨海默病,就是“老年痴呆症”中最为常见的一种。目前全球至少5000万痴呆症患者,预计到2050年,这个数字将达到1.52亿,而其中70%左右均为阿尔茨海默病患者。
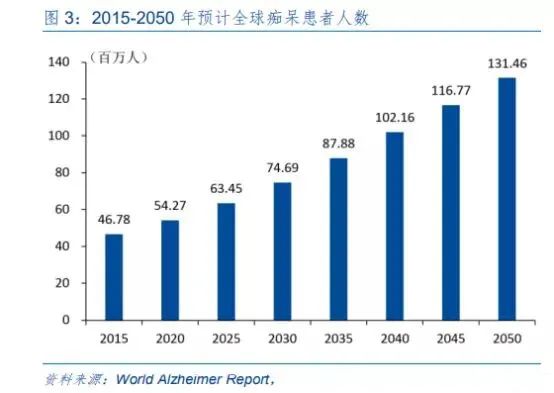
这意味着,在百岁人生的时代,超过一半人,都要面对阿尔茨海默病的问题。
然而令人沮丧的是,这种病却几乎无法治疗,现有的药物只能暂缓认知衰退,无法抑制病情发展,迄今为止,人类发明的绝大多数针对阿尔茨海默病的药物研究,都以失败告终。
全球科学家都在致力寻找有效的药物,而一篇发表于国际学术期刊《Advanced Science》上的文章表示:脐带间充质干细胞(hUC-MSCs)具有修复损伤神经细胞的功能,能够通过HGF-cMet-AKT-GSK3β通路调节tau蛋白磷酸化,显著提高阿尔茨海默病模型动物的学习记忆和认知能力。

△ HGF介导临床级人脐带间充质干细胞改善功能恢复在衰老加速的阿尔茨海默病小鼠模型中
众多临床试验也表明,干细胞移植治疗阿尔茨海默病不仅能够调节脑内炎症性环境,而且促进神经再生和突触链接,有效改善病症,且安全无副作用。
或许,解决阿尔茨海默病治愈难问题,干细胞将会是个不错选择。
“温柔的绝症”阿尔兹海默病
阿尔茨海默病(Alzheimer’s disease,AD)是我们俗称为“老年痴呆症”中最常见的一种,是一种发病进程缓慢、随着时间不断恶化的神经退化性疾病,多发生于老年和老年前期,尤其是65岁以上老人,占到95%的比例。
也就是说,每10个老人,就有1个得上这种病。
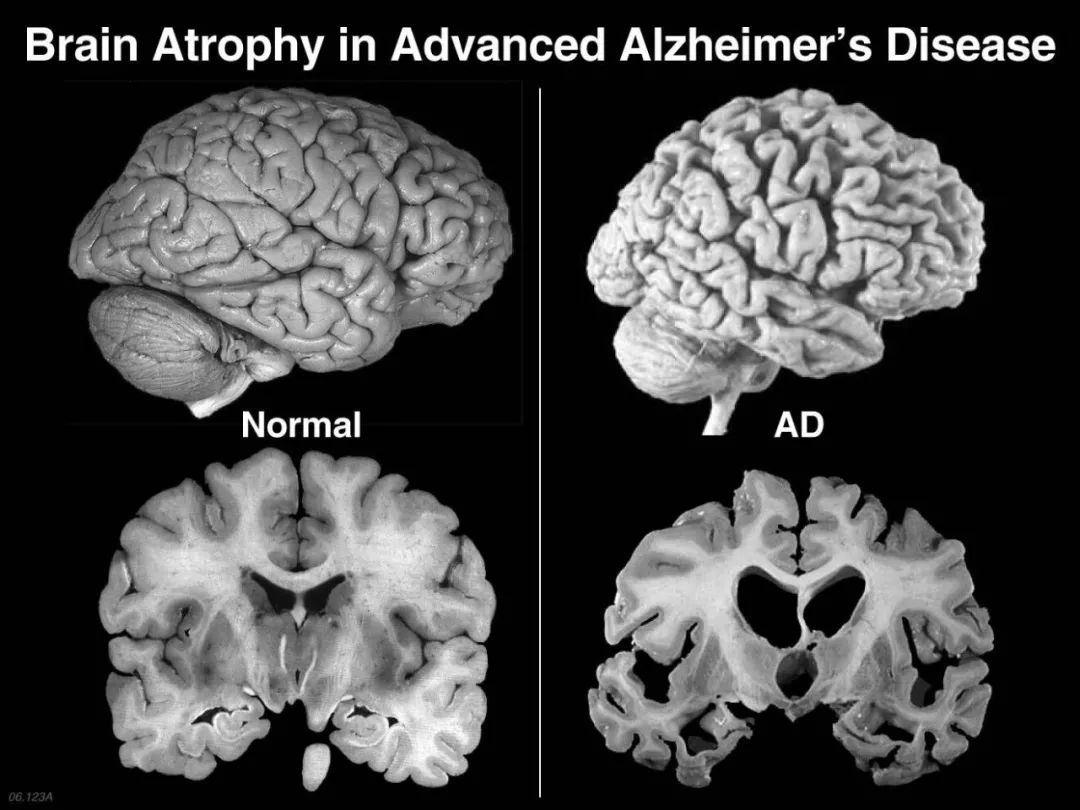
△ 大脑受损是阿尔茨海默病发生的原因
不仅如此,一些研究发现,其实痴呆症状早在十多年前就出现了!
临床上最年轻的患者大概在三十几岁,其实这也是阿尔茨海默病在早期发病的表现,很多患者的大脑早在十多年前就已经开始发生变化,随着病情进展,患者首先出现认知功能衰退,然后出现情绪和行为问题。当病情发展到一定程度后,患者会逐渐丧失身体机能,最终死亡。

当然,这种疾病之所以可怕,还因为它会缓慢剥夺一个人的能力,尊严和生命。它带给人们的痛苦不仅是物理的痛苦,而是更加深层的理性的痛苦。
他们就像脑海中有个橡皮擦,擦掉亲朋好友,慢慢地,也会丢掉基本的生存能力。
最后,这种疾病在晚期会给家人带来很大的经济,生活和情感压力。一些照护家人因此而变得焦虑、忧郁、或发生其他的疾病。
但目前科学家仍未找到引起阿尔茨海默病的根本原因,更绝望的是,连能治疗的药物都没有,也就是说,面对这个疾病,患者跟家人根本不知道到底该怎么办。

干细胞给老年痴呆“一线生机”
虽然病因不明,但衰老无疑是导致阿尔茨海默病的主要原因。
随着年龄增长,大脑神经开始进行性退化,其特征就是神经元丧失和认知能力下降,有研究表明,阿尔茨海默病患者的神经和突触损失是该病症的两个标志性病变,也就是淀粉样蛋白β含斑块和神经原纤维缠结(NFTs的),这是由微管相关蛋白tau的高磷酸化形式。
而干细胞,尤其是间充质干细胞(hUC-MSC)保持较早的胚胎发育阶段,更年轻、产量更高,可以分泌多种功能因子,在多种疾病治疗中都展现了广阔的临床应用价值。
研究人员建立了基于hUC-MSC的对SAMP8小鼠认知能力恢复的影响,该模型是阿尔茨海默病衰老加速小鼠模型。
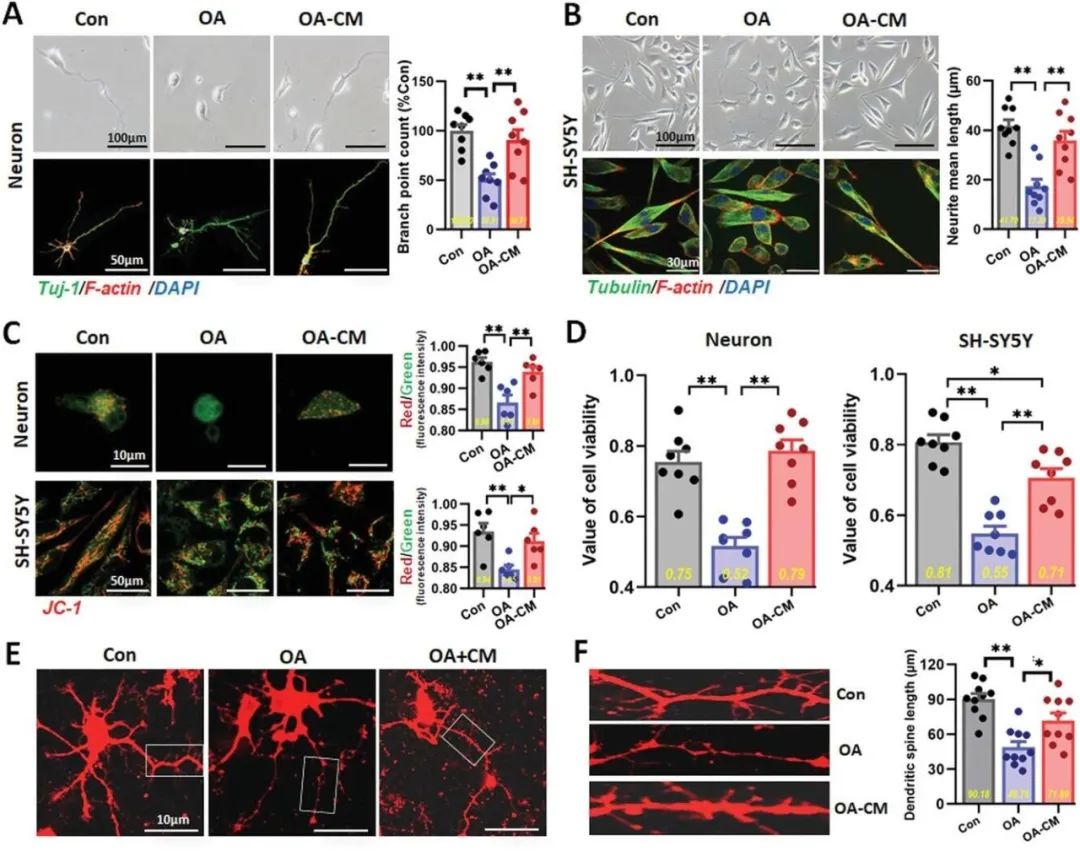
△ hUC-MSC在体外AD细胞模型中恢复了OA诱导的神经细胞损伤
研究证明,临床级hUC-MSC的腹膜内给药可以抵消老年小鼠的突触可塑性、神经网络、分子调控和认知的衰老。这些作用表明hUC-MSCs可能是系统性调节衰老大脑并介入认知衰老的生理过程的首选资源。
更重要的是,hUC-MSC可以分泌多种功能因子,包括生长因子、细胞因子、趋化因子和代谢产物。
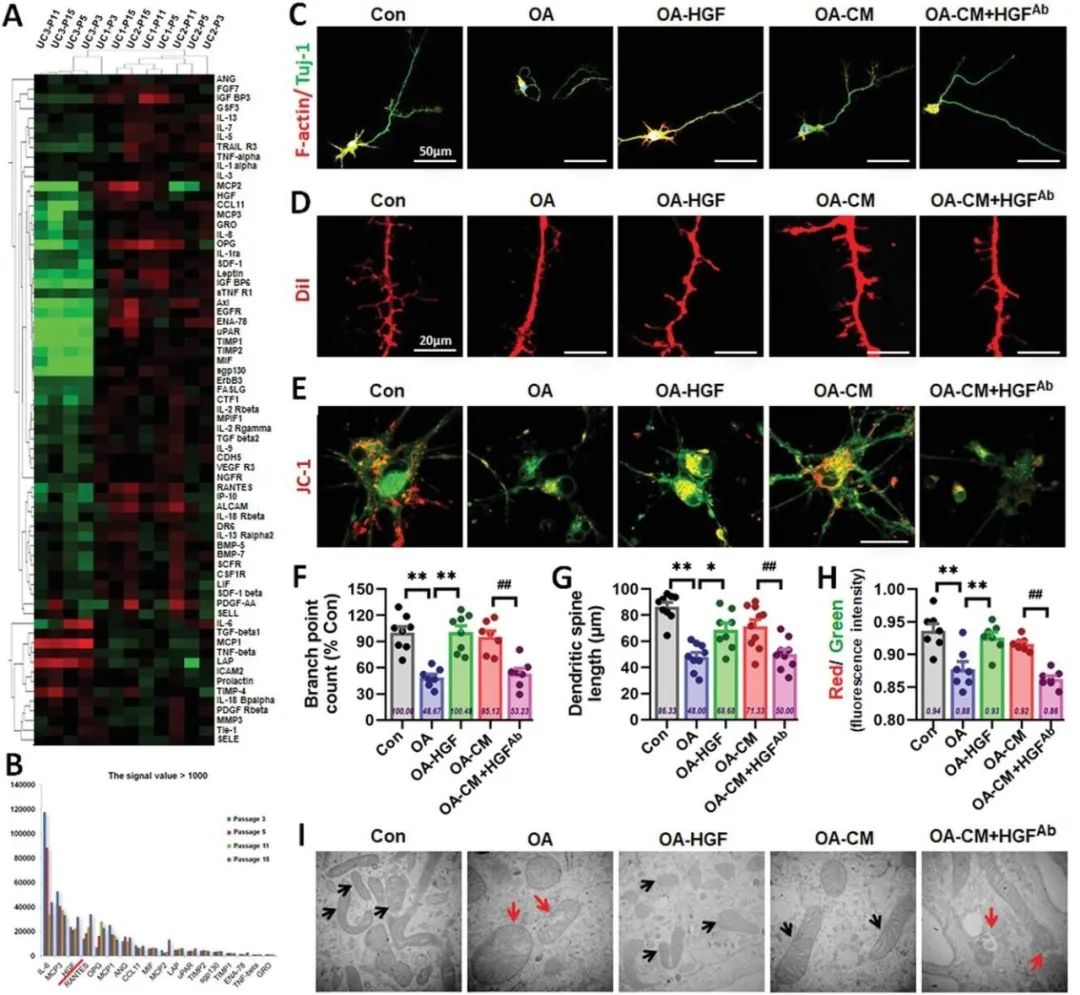
△ hUC-MSCs分泌的HGF可以从OA诱导的神经细胞损伤中拯救AD细胞模型
该项研究首次探索了临床级hUC-MSC对SAMP8小鼠认知能力恢复的影响,并且证明了hUC-MSC分泌的核心功能因子肝细胞生长因子(HGF)通过下调tau蛋白的过度磷酸化,改善神经原纤维缠结,逆转脊柱丢失,在hUC-MSC调节受损神经细胞的恢复中起着重要作用。
并且,hUC-MSC也促进了老年小鼠大脑中的神经突触链接,这些都是与记忆缺陷密切相关的。
干细胞治疗阿尔茨海默病的机制
近年来,AD研究中最常用的细胞是胚胎干细胞(ESCs),间充质干细胞(MSCs),神经干细胞(NSCs)和诱导多能干细胞(iPSC)。
干细胞治疗阿尔茨海默病的机制为:
分化成神经样细胞
干细胞可自我复制及产生神经组织细胞。移植后干细胞可分化成AChE神经元,与宿主功能整合、形成神经环路,替代AD病程中丢失的细胞。研究证实,成活的干细胞更多地分化成神经胶质,通过不同途径在退行性疾病中发挥作用。
分泌营养因子
研究人员发现,移植后NSCs只有约5%分化为成熟神经元,并且随后其周围细胞未凋亡,且与其他细胞连接更密集,可见NSCs挽救小鼠记忆可能主要是分泌神经营养素阻止脑细胞凋亡,并增强神经元之间相互联系,维持大脑功能。
促进内源性修复
研究证明:BM-MSCs移植治疗脑卒中大鼠后,内源性NSCs增殖活跃。干细胞移植后,刺激固有的NSCs增殖,并诱导分化成神经组织细胞替代缺损细胞,即启动内源性途径修复损伤。内源性NSCs更具优势,诱导其增殖并分化为神经元形成功能网络,是AD治疗的研究方向。
刺激血管再生
在实验中,移植BM-MSCs治疗心血管疾病,移植后bFGF、PDGF、VEGF、血管生成素分泌上调,促进血管内皮和平滑肌细胞增殖。主流观点认为,干细胞移植治疗心血管疾病主要在于干细胞旁分泌生物活性因子,诱导血管生成,保护组织。这对AD和血管型痴呆的干细胞移植治疗有一定启示。
作用于炎性细胞
炎性反应在退行性疾病中的作用已得到认同。干细胞移植治疗中枢神经系统疾病,常伴有移植后小胶质细胞功能活跃。小胶质细胞属于单核吞噬细胞系统,主要功能是吞噬病灶周围浸润的炎性细胞。干细胞移植后还可以分泌一些细胞黏附分子,表现出免疫样功能。
干细胞具有多向分化、组织再生、调控免疫的功能,在多种退行性疾病的治疗中都展现了良好的临床疗效,相信未来随着再生医学的不断发展,阿尔茨海默病、帕金森、脑中风等这类严重影响老年人生活质量的疾病,都能被干细胞攻克,至少能够缓解病症,提高患者生活质量,为更多老年人带来福音。
-END-
素材源于网络,内容有改动
版权归原作者所有,侵删!
【北联世纪干细胞】
— 感谢 · 阅读 —
北京北联世纪干细胞生物科技有限公司,是一所集临床、科研、国际学术交流为一体的全球生命科学研究公司,技术源头为美国圣地亚哥Biocentrium公司,公司致力于再生医学新技术的基础研究与临床应用转化,并将iPSc诱导多能干细胞培养技术平移到国内,同时与国内多家三甲医院开展科研课题。
现涵盖iPSc诱导多能干细胞,鲜活细胞、间充质干细胞、神经干细胞、血管内皮干细胞、软骨干细胞、NK/NKT/CTL/CAR-T/CAR-NK/DC-CIK/INKT等免疫细胞,肿瘤疫苗等;应用范围包括:疾病预防、两性生殖、神经系统疾病、脑部疾病、亚健康、免疫系统疾病、骨关节疾病等,同时拥有个体化iPS制备和分化成精原细胞、卵原细胞并形成精子、卵子技术、NSC脑部立体定向技术、NSC球后视神经靶向技术等。




